2022年10月16日�,國家醫(yī)保局發(fā)布《關(guān)于2022年國家醫(yī)保藥品目錄調(diào)整通過形式審查的申報藥品專家評審階段性結(jié)果的公告》��,意味著2022年度國家醫(yī)保談判專家評審工作已完成。
早前6月29日��,國家醫(yī)保局發(fā)布《2022年國家基本醫(yī)療保險�����、工傷保險和生育保險藥品目錄調(diào)整工作方案》及相關(guān)文件,標志著第五輪國家醫(yī)保藥品目錄調(diào)整工作正式啟動�����。其中��,專家審評階段與2021年相比����,主要內(nèi)容變化如下:
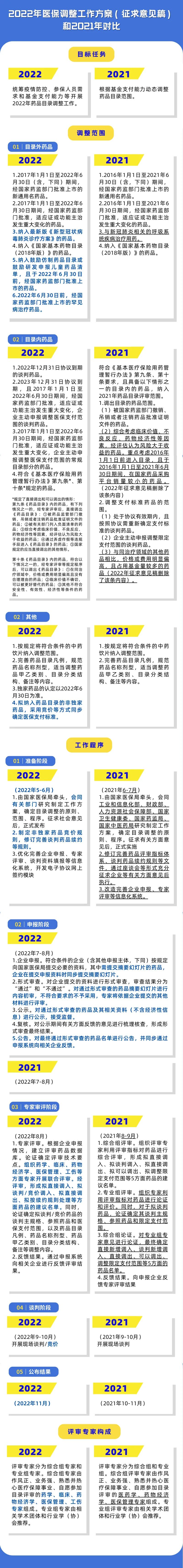
343個藥品通過形式審查,談判在即
9月17日��,國家醫(yī)保局公布了《2022年國家基本醫(yī)療保險�、工傷保險和生育保險藥品目錄調(diào)整通過形式審查藥品名單的公告》,與9月6日公布的通過初步審查名單相比略有調(diào)整�,目錄外藥品甲硝維參陰道膨脹栓被移除,共343個藥品通過形式審查�����。
根據(jù)文件���,今年的醫(yī)保目錄調(diào)整程序仍分為準備��、申報��、專家審評�、談判和公布結(jié)果五個階段�。值得關(guān)注的是,醫(yī)保局進一步優(yōu)化了企業(yè)申報的內(nèi)容����,豐富了申報資料中對藥品提交信息的要求,包括有效性��、安全性��、經(jīng)濟性����、創(chuàng)新性和公平性等,并請企業(yè)提交藥品信息摘要幻燈片�����,給予企業(yè)更多機會向?qū)<医榻B自己的品種�����。目前專家審評工作已經(jīng)結(jié)束,意味著備受矚目的談判階段即將到來���,按照公告顯示的企業(yè)提交材料截止日期11月3日預估�,談判或?qū)⒃?1月進行��。
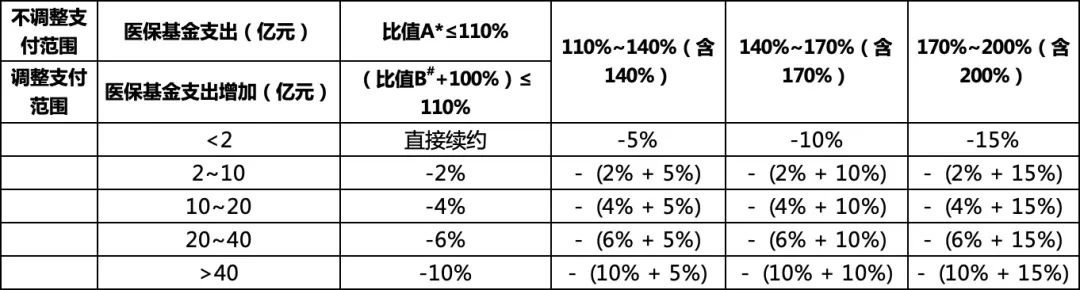
名單內(nèi)藥品亮點十足
此次通過形式審查的343種藥品�����,包括目錄外新增品種西藥183個��、中成藥15個����;目錄內(nèi)續(xù)約品種西藥111個、中成藥34個���。通過梳理發(fā)現(xiàn)�,本輪醫(yī)保談判依舊看點十足����。
1、向罕見病��、兒童藥傾斜
與此前醫(yī)保目錄調(diào)整相比,本輪調(diào)整向罕見病和兒童用藥傾斜�。具體體現(xiàn)在對罕見病藥品的申報沒有設(shè)置“2017年1月1日后批準上市”的限制。兒童用藥方面�����,與2021年相比����,增加了“納入鼓勵仿制藥品目錄或鼓勵研發(fā)申報兒童藥品清單�,且于2022年6月30日前經(jīng)國家藥監(jiān)部門批準上市的藥品”可以申報醫(yī)保目錄。據(jù)統(tǒng)計��,今年通過形式審查的名單中有19種罕見病藥物�。據(jù)GBI此前發(fā)布的專題報告(點擊相關(guān)閱讀),2021年共有7個罕見病藥新增談判成功�����,適應證涉及法布雷病�、B型血友病、遺傳性血管性水腫(HAE)��、純合子型家族性高膽固醇血癥(HoFH)���、脊髓性肌萎縮癥(SMA)�、蛋白淀粉樣心肌病和多發(fā)性硬化。其中渤健旗下SMA治療藥諾西那生鈉以33000元/針左右的價格進入醫(yī)保覆蓋�����,以單價55萬為基準降幅高達93.97%���。今年罕見病藥物談判將有哪些新的突破�����,值得期待����。
2�、“天價”CAR-T再引關(guān)注
本次藥明巨諾旗下瑞基奧侖賽注射液(倍諾達)也在名單中,倍諾達是藥明巨諾自主開發(fā)的一款靶向CD19的自體CAR-T細胞免疫治療藥物����,于2021年9月1日獲批在中國上市,它是繼復星凱特阿基侖賽注射液(商品名:奕凱達)之后國內(nèi)第二款獲批的CAR-T療法����。去年奕凱達也在273個通過形式審查的藥品名單中�����,但是由于其高昂的售價(120萬/針)不符合醫(yī)保談判“?��;?rdquo;的原則,不具備經(jīng)濟性����,因此最終未能獲得安排資格��。129萬/針的倍諾達今年的命運將如何�����?能否開創(chuàng)“天價”藥品進入醫(yī)保目錄的先河����?11月見分曉。
3��、腫瘤藥數(shù)量最多����,國產(chǎn)PD-1適應證大戰(zhàn)
本次跨國藥企旗下PD-(L)1藥品未出現(xiàn)在名單中����,相關(guān)“廝殺”將在國內(nèi)藥企中展開�。其中,恒瑞醫(yī)藥卡瑞利珠單抗新增4項適應證��;君實生物特瑞普利單抗新增2項適應證����;信達生物信迪利單抗新增2項適應證;百濟神州替雷利珠單抗新增4個新適應癥和1個目錄內(nèi)適應證的新聯(lián)用方案�����。此外�����,復宏漢霖PD-1斯魯利單抗�����、康寧杰瑞/思路迪/先聲藥業(yè)PD-L1恩沃利單抗��、康方生物PD-1/CTLA-4雙抗卡度尼利單抗也在名單中。在新晉者加入后���,PD-(L)1的競爭局面將如何�����?讓我們共同期待���。
4、新冠口服藥或?qū)⒄竭M入醫(yī)保���?
另外值得關(guān)注的是��,國產(chǎn)新冠口服藥阿茲夫定片和輝瑞Paxlovid(奈瑪特韋片/利托那韋片)也出現(xiàn)在通過形式審查的名單中。其中��,阿茲夫定的藥品信息顯示申報適應證為高病毒載量的HIV-1感染��。阿茲夫定片系我國自主研發(fā)的口服小分子藥物�����,分別于2021年7月和2022年7月獲批HIV和COVID-19適應證��,復星醫(yī)藥擁有該藥部分區(qū)域的獨家商業(yè)權(quán)益���。2022年8月�����,阿茲夫定被納入第九版新冠診療方案����。Paxlovid是口服小分子新冠病毒治療藥物,于2022年2月經(jīng)國家藥監(jiān)局附條件批準進口注冊�����,同年3月首批21200盒Paxlovid進入中國�����,采購價為2300元/盒��,并納入臨時醫(yī)保��。此次談判Paxlovid能否正式進入����?值得關(guān)注。
文章來源:GBIHealth